해양미생물유래 천연물 연구 국제동향
- 조회 : 23785
- 등록일 : 2017-07-31
『해양미생물유래 천연물 연구 국제동향』
해양생명공학연구센터 신희재 책임연구원
1. 서론 (배경)
세계 의약품 시장의 규모는 1,200조1)
정도로서, 세계적인 경기침체에도 불구하고 연평균 6~8% 정도의 꾸준한 성장세를 이어가고 있다. 이러한 세계 의약품 시장의 급격한 확대는 세계적인 인구고령화 추세에 따라, 치매, 중풍, 파킨슨병 등 노인성질환의 증가 및 고혈압, 당뇨 등의 만성질환에 대한 치료 수요가 빠르게 증가하고 있기 때문이다. 전 세계적으로 보건·의료, 식량, 에너지, 환경변화 등 인류의 난제에 직면하면서 해양바이오는 이를 해결할 핵심영역으로 각광을 받고 있다. 현재 시판되고 있는 의약품의 약 40~50% 정도가 생물자원에서 분리된 천연물이거나 천연물에서 유래된 물질이다(Newman and Cragg, 2016). 신약개발을 위한 천연물화학 분야에서 육상 식물 및 미생물은 가장 중요한 자원들이다. 세계 최대의 바이오제약 전시회인 '바이오 인터내셔널 컨벤션(바이오 USA)2) BIO International Convention(BIO USA).
'에서 2017년에 가장 주목받는 분야는 ‘미생물을 약으로(Bugs as drugs)’로서 바이오산업계에 새로운 영역이 출현하고 있다. 미생물은 적은 투자비용으로 천연물, 유전자, 단백질 정보 등을 확보할 수 있는 생명공학 산업의 핵심소재 중의 하나인 고부가가치 자원이다. 또한 산업적으로는 세계 바이오시장의 30%, 국내 바이오산업의 60%를 차지하고 있을 만큼 산업과 연관이 아주 크다. 현재까지 미생물로부터 약 70,000종 정도의 천연물이 분리되었으며, 그 중에 500종 정도가 의약품으로 개발되었다(Berdy, 2012). 이와 같이 미생물로부터의 높은 의약품 개발 빈도 때문에 현재까지 육상미생물에 대한 많은 연구가 이루어져왔으며 새로운 천연물을 찾기가 어려워, 신규 천연물 발굴을 위한 새로운 미생물 자원의 탐색이 세계적으로 이루어지고 있다. 그중에서도 가장 각광을 받고 있는 미생물 자원은 해양미생물과 인간의 체내에 살고 있는 장내 미생물군(마이크로바이옴)3)이다. 최근 장내 미생물은 알레르기나 비염, 아토피, 비만, 우울증, 치매, 각종 대사ㆍ면역질환, 장염, 심장병, 암과도 관련된 것으로 보고되고 있다. 생명과학분야에서 세계 최고의 학술지 중의 하나인 ‘Cell’지는 2013년 1월에 장내 미생물을 활용한 신약개발 연구를 표지논문으로 소개했으며 'Science'지는 장내 미생물과 사람의 건강에 관련한 연구 결과를 '2013년 10대 과학 뉴스'의 하나로 꼽았다. 또한 세계경제포럼에서는 인간의 장내 미생물을 이용한 질병치료 및 신약개발을 ‘2014년 10대 유망기술’에 선정하였을 만큼 세계적으로 주목을 받고 있다. 이 같은 장내미생물에 쏟아지는 관심을 입증하듯 오바마 미국 행정부는 2016년 임기 마지막 과학 프로젝트로 “National Microbiome Initiative”를 발표했으며, 막대한 연구비를 투입하고 있다(Bouchie, 2016). 한편 해양미생물은 육상미생물과 달리 높은 염분, 수압, 저온 등의 특수한 해양환경에서 진화를 거듭해 오며 생존을 위해 육상미생물과는 다른 다양한 2차대사물질들(secondary metabolites)을 만들고 있는데 이러한 물질들이 지금까지 개발된 의약품과는 다른 구조와 성질을 가지고 있어 의약품 개발에 있어 상당한 기대를 모으고 있다. 또한 현재 사용되고 있는 대부분의 항생제들은 육상미생물로부터 개발되었으나, 항생제에 저항성을 가지는 내성균들이 출현하면서 세계적으로 큰 문제가 되고 있다. 이러한 항생제 내성균 및 다양한 질환을 치료할 수 있는 대안으로서 해양미생물로부터 유래된 천연물들(Marine Microbial Natural Products)이 각광을 받고 있다. 따라서, 세계 각국은 해양미생물들이 생산하는 신규 천연물들의 탐색 및 의약품 개발 관련 기술 확보를 위하여 활발한 연구를 진행하고 있다.
1) The Global Use of Medicines: Outlook through 2017, IMS Institute for Healthcare Informatics.
2) BIO International Convention(BIO USA).
3) Microbiome: 우리 몸속에 공존하는 장내 미생물의 유전정보 전체.
2. KIOST 관련 연구사업 소개
2.1 필요성
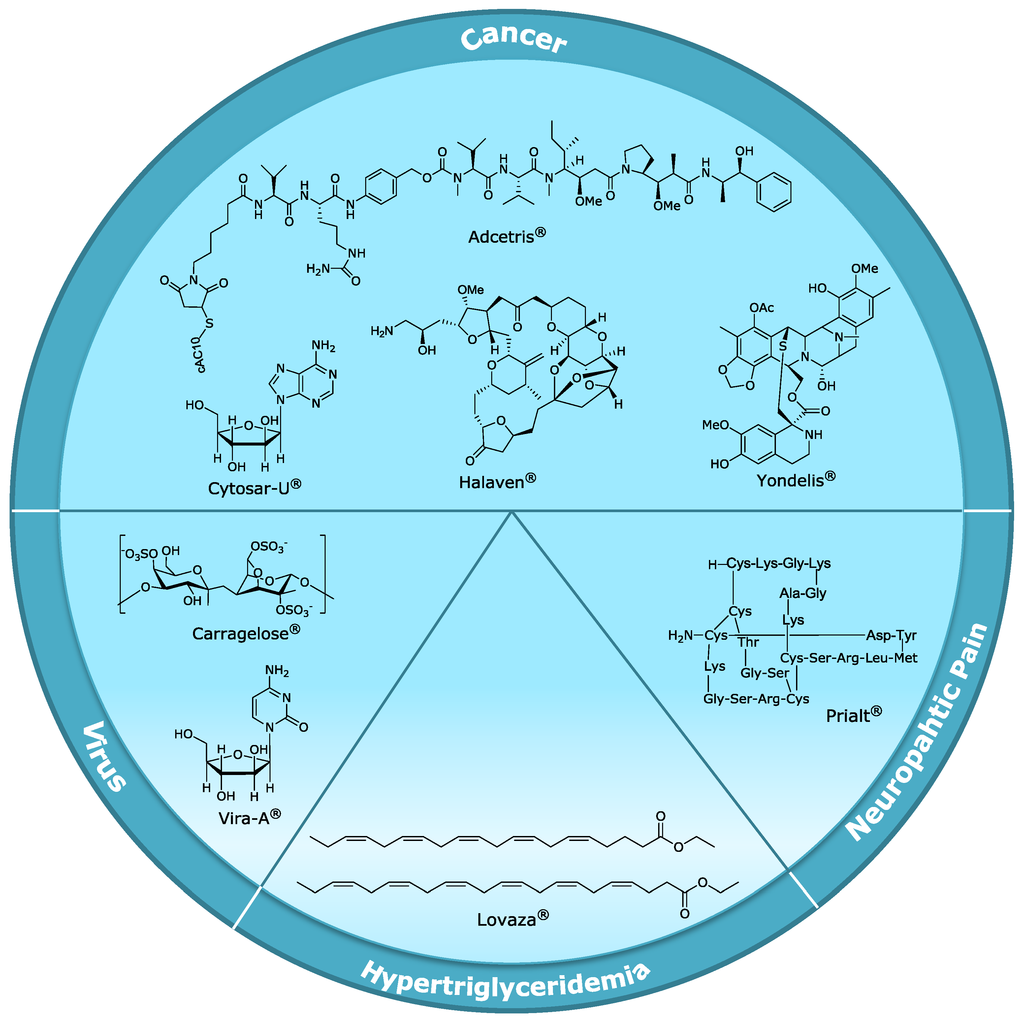
해양은 지구 전체의 약 70%를 차지하며, 지구상에 존재하는 생물의 80% 이상이 서식하고 있는 생물다양성의 보고이다. 해양은 극한 환경이면서도 복잡하고도 다양한 환경을 가진다. 해양 환경의 특수성과 천연물개발의 원천으로서의 해양생물의 뛰어난 가치로 말미암아, 육상천연물 연구에 비해 훨씬 짧은 연구기간에도 불구하고 육상생물 유래의 생리활성 물질과는 다른 독특한 구조를 가진 20,000종 이상의 생리활성물질이 해양생물로부터 분리되었으며 이들 물질은 생리활성 면에서도 뛰어난 모습을 보여주었다(McCarthy, 2004). 현재 해양생물로부터 개발된 의약품에는 항암제들인 adcetris®, cytosar-U®(Ara-C, cytarabine, depoCyt), halaven®, yondelis®, 항바이러스제인 vidarabine(Ara-A®), 고중성지방혈증 치료제인 lovaza®, 진통제인 prialt® 등이 전문의약품으로서 개발되어 있고, 감기치료약인 carragelose가 일반의약품으로 시판되고 있다(Martins et al., 2014).
|
그림 1. 해양천연물로부터 개발된 의약품들. |
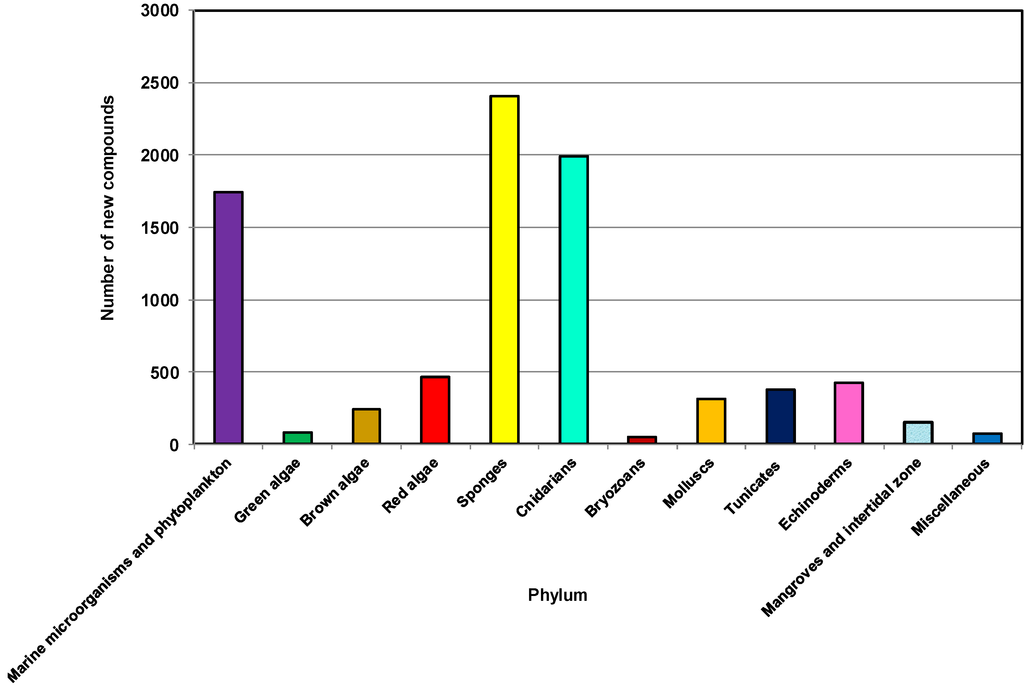
해양생물로부터 의약품 개발에 있어서 가장 큰 문제점은 해양생물체내에서의 활성물질의 농도가 매우 낮아 활성물질을 대량분리, 정제하여 의약품개발에 필요한 충분한 양을 공급하기가 어려운 문제(supply problem)이다. 해양생물에서 가장 많은 신물질이 분리된 분류군은 해면동물이나 자포동물과 같은 무척추동물(그림 2, Mehbub et al., 2014)이지만 이런 생물의 채집은 주로 스쿠버다이빙에 의존하기 때문에 시료의 대량 확보나 재채집이 어려우며, 대량양식 또한 무척 어렵다. 또한, 일반적으로 해양천연물의 구조가 복잡하여 합성에 의하여 활성물질을 대량생산하는 것은 대부분의 경우 매우 어렵거나 가격경쟁력에서 상업화에 적합하지 않다. 그러나 해양미생물의 경우, 육상미생물 이상의 다양한 구조와 활성을 가지는 신물질들을 많이 생산하며, 배양을 통해 의약품 개발에 필요한 양을 지속적으로 공급할 수 있기 때문에 새로운 의약품개발을 위해서 해양미생물을 체계적으로 탐색하고 유용 천연물을 발굴하는 것이 필요하다. 나고야의정서4) 의 발효로 국가 간에 갈수록 치열해지는 해양생물자원의 확보 경쟁 속에서 우리나라의 해양생물 주권 확보에 기여하고 해양바이오 산업 발전에 큰 역할을 할 해양미생물의 확보/보존 및 이들이 생산하는 천연물의 실용화 기반 구축을 위한 연구개발사업의 지속적인 수행이 필요하다.
|
그림 2. 해양생물 분류군별 분리된 신물질의 갯수(2001-2010년). |
2.2 주요내용
한국해양과학기술원(한국해양연구원)에서는 2003년부터 해양수산부(국토해양부)의 ‘해양과학기술연구개발사업’ 및 기타 연구사업의 일환으로서 “해양방선균으로부터 항암물질 개발”사업(2003~2008, 연구책임자 신희재)과 “해양생물로부터 항노화 바이오소재 개발 연구”사업(2012~2014, 연구책임자 신희재), “해양자원유래 고령친화형 글로벌 기능성 식품소재 개발”사업(2017~, 공동연구책임자 신희재) 등 해양미생물로부터 유용 천연물 발굴 사업을 진행해오고 있다. 이러한 연구사업들의 주된 연구목표는 국내에서의 독자적인 해양신물질 개발역량을 확보하기 위하여 해양미생물의 분리 및 체계적인 보존, 배양, 생리활성 해양천연물의 분리정제, 신물질의 구조결정, 활성의 검색, 신규 활성유도체의 합성, 작용기전의 규명, 동물실험을 통한 활성검증 등의 기술수준을 선진국 수준으로 향상시키려는 기술적 목표와, 해양미생물로부터 선도물질의 도출 및 이를 효율적으로 대량생산할 수 있는 방법을 연구하여 실용화의 기반을 구축하는 산업적인 목표를 함께 추구하고 있다.
2.2.1. 해양미생물의 분리 및 보존
한국해양과학기술원은 국가의 중요한 생물자원이며 미래자산이 될 해양미생물을 분리하기에 최고의 인프라를 가지고 있다. 해양은 광대하고도 다양한 생물학적 환경을 가진다. 해양과기원에서는 열대지방인 마이크로네시아의 축(Chuuk)에 연구기지를 가지고 있으며, 남극에 세종기지 및 장보고기지와 북극에 다산기지를 가지고 있다. 또한 심해연구를 위한 무인잠수정 해미래와 6천톤급 연구선 이사부호를 보유하고 있다. 이러한 기지와 연구인프라를 활용하여 열대지방, 극한지, 심해 등으로부터 다양하고도 특이한 해양미생물들을 분리하여 보존하여 왔다. 또한 국내에 이어도 및 가거초 종합해양과학기지와 울릉도ㆍ독도 해양과학기지, 남해연구소, 동해연구소 등의 연구 인프라를 갖추고 있어서 다양한 해양시료들을 안정적이고 지속적으로 확보할 수 있으며, 이러한 시료들로부터 다양한 해양미생물을 체계적으로 확보, 보존하고 있다.
4) Nagoya Protocol: 생물(유전)자원에 대한 접근 및 그 이용으로부터 발생하는 이익을 제공국과 이용 국가 간에 공유하기 위한 지침을 담은 국제협약.
2.2.2. 해양미생물로부터 유용 신물질의 발굴
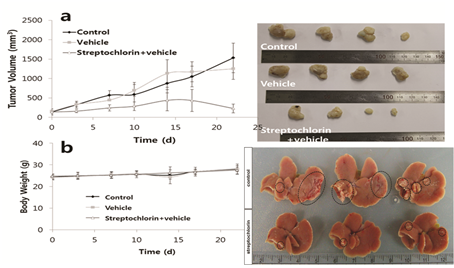
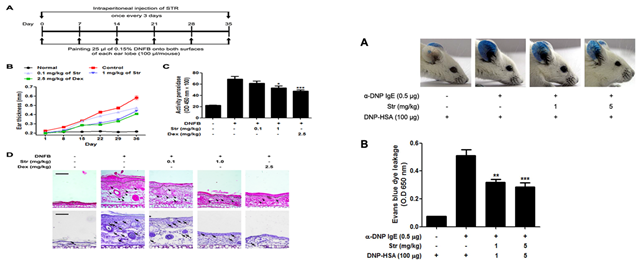
지금까지 분리된 다양한 해양미생물들을 소량배양하여 에틸아세테이트와 같은 유기용매로 추출하여 추출물 라이브러리를 구축하였고, 항균, 항암, 항염 등의 활성 검색을 통하여 우수한 활성을 보이는 균주를 1차적으로 선별하였다. 또한, 활성 검색결과와 함께 화학적 분석 및 균주의 배양학적, 형태적 특성 등을 종합적으로 고려하여 연구대상 유용균주를 최종적으로 선정하였다. 선정된 유용 해양미생물 균주를 발효기를 이용하여 대량배양한 시료로부터 활성물질을 분리, 정제 하였다. 분리된 물질들의 구조는 각종 분광학적 방법과 화학적 방법에 의하여 규명하였고, 지금까지 200여종의 신물질들을 발굴하였다. 이들 물질들은 알칼로이드, 펩타이드, 이소프레노이드, 터핀노이드, 마크로라이드, 폴리키타이드 등의 여러 가지 분류군에 속하며 다양하고도 특이한 구조를 가지는 신물질들을 얻을 수 있었다. 이들 중에서 많은 물질들이 항암, 항염, 항균, 항알러지 등의 뛰어난 활성을 나타내었다. 예로서, 동해안의 아야진에서 분리한 해양방선균 스트렙토마이세스(Streptomyces)에서 분리한 스트렙토클로린(streptochlorin)이라고 명명한 물질은 분자량이 아주 작고 특이한 구조를 가지고 있으며, 뛰어난 활성을 가지고 있기 때문에 기전연구 및 동물실험을 진행하기 위하여 전합성을 수행하여, 짧은 합성 단계로 이 물질을 대량합성 할 수 있는 방법을 개발하였다. 스트렙토클로린은 동물실험에서도 강력한 항암활성(그림 3) 및 항알러지 활성(그림 4)을 나타내었다. 스트렙토클로린은 대조군으로 사용한 미국 식품의약국(FDA)로부터 승인을 받은 의약품인 덱사메타손(dexamethasone)보다 2.5배 낮은 농도에서도 거의 동등한 항알러지 및 항염 효과(그림 4)를 나타내어 향후 아토피, 천식, 비염, 피부염과 같은 알러지성 질환에 대한 선도물질로서의 개발 가능성을 충분히 가지고 있음을 알 수 있었다.
|
그림 3 동물실험에서 스트렙토클로린의 담관암 억제 효능. |
또한 이어도 해양과학기지 주변의 해양퇴적토에서 항균활성을 가지는 Bacillus 속 해양미생물을 분리하고, 이 미생물의 대량배양액으로부터 지금까지 전혀 보고된 적이 없는 특이한 구조를 가지는 신규 항생물질을 분리하여 그 구조를 규명하고, 이들 신물질의 이름을 이어도의 명칭을 따서 “이어도마이신(ieodomycin)”, “이어도글루코마이드(ieodoglucomide)”, “이어도글루코리피드(ieodoglucolipid)” 등으로 명명하고 국제저널에 다수 투고하여 이어도가 대한민국 영토임을 국제적으로 널리 알리는데도 기여하였다. 이들 신규 항생물질은 다양한 세균들에 대하여 강력한 항균활성을 가지고 있어서 향후 항생물질로의 개발 가능성이 아주 크다. 특히 이어도마이신은 지금까지 가장 많이 팔린 의약품인 고지혈증치료제인 리피토, 심바스타틴과 같은 스타틴(statin) 계열의 의약품과 구조적인 유사성을 가지고 있으나, 훨씬 간단한 형태를 취하고 있어 고지혈증 치료제로서의 개발 가능성이 높아 현재 전합성 연구를 진행하고 있다. 마이크로네시아에서 분리한 해양미생물 Bacillus sp. 102CH635-3 균주가 생성하는 pantetheine계 신규물질은 뛰어난 항염 활성 및 발모촉진 효과를 가지고 있었다. 이들 신규물질을 용이하게 얻기 위하여 간단한 단계의 합성반응으로 pantetheine계 신규물질을 전합성할 수 있는 효과적인 대량합성법을 개발하였으며, 유기반응을 통하여 pantetheine계 신규물질의 유도체들도 합성하였다. 또한 신규 유도체에 대한 항염활성을 검색하여 구조-활성 상관관계를 파악하였다. 가거초에서 분리한 해양미생물 Bacillus subtilis로부터 가거테트린(gageotetrin)이라고 명명한 3종의 신규 항진균 물질을 분리하고 구조를 규명하였다. 이 물질들은 지질펩타이드(lipopeptide)성 물질로서 아미노산과 신규 지방산으로 구성된 아주 특이한 구조를 하고 있었으며, 전 세계적으로 고추, 가지, 오이 등의 농작물에 막대한 피해(국내 1,000억원/년 추정)를 입히는 식물 병원균인 Phytophthora capsici에 대하여 아주 낮은 농도(0.02 μM)에서도 강력한 항진균 작용을 나타낼 뿐만 아니라 병원균의 운동성을 저해하며 용균작용까지 가지는 특이한 작용기전을 가지고 있음을 밝혔다. 이 신물질들은 항진균제로 개발된 지질펩타이드인 카스포펀진(caspofungin)보다 훨씬 간단한 구조를 가지면서도 강력한 항진균 작용과 독특한 작용기전을 가지고 있으며, 식물병원균 이외에의 균들에도 강력한 항균작용을 가지고 있어, 향후 항진균제 및 항균제 개발에 있어서 선도물질로서 충분한 개발 가능성을 가지고 있음을 알 수 있었다.
|
그림 4. 스트렙토클로린(Str)의 알러지 억제 효능. |
2.2.3. 연구결과의 시사점
전술한 다양한 신규물질 이외에도 항생제 내성균에 대해 뛰어난 항균작용을 나타내는 신물질 및 치매, 당뇨 등에 효과를 나타내는 다양한 신물질을 해양미생물로부터 발굴하였다. 이러한 연구결과를 통하여 해양미생물로부터 천연물 신약개발의 가능성이 충분히 높음을 알 수 있었다. 또한,해양신물질 개발을 위한 기술적 기반을 확립하고 몇몇 신물질의 향후의 산업화를 위한 활성물질의 합성법을 개발하였고, 다양한 해양미생물 및 천연물 소재를 확보하였다. 그러나 개발 가능성이 높은 다양한 신물질을 발굴하였음에도 불구하고 지속적인 연구비 확보의 어려움 때문에 논문투고나 국내 특허출원으로 연구결과를 마무리 하는 경우가 대부분이었다. 천연물 신약개발 연구는 많은 시간과 대규모 연구비가 소요되는 장기 연구프로젝트이다. 신약개발은 원천생물 확보, 활성물질 탐색, 선도물질 발굴, 후보물질 도출, 임상연구 등의 많은 단계를 넘어야 도달할 수 있는 지난한 과정이며, 그 결과로 엄청난 경제적, 과학적인 파급효과를 가져오는 연구이다. 많은 가능성을 가지고 있는 신물질들이 사장되지 않게 다음 단계를 넘을 수 있도록 정부의 지속적인 지원이 절실히 필요하다.
3. 국제동향
3.1 주요 쟁점별 논의 동향
해양미생물 유래의 신약개발 연구를 위해 가장 선결되어야 될 과제는 우수한 미생물 자원을 발굴하고 선점하는 일이다. 선진국에서는 새로운 의약소재를 개발하기 위해 유용 해양미생물 발굴을 위한 생물자원탐사(bioprosepcting)를 활발히 진행하여 왔다. 세계 최초로 '인간 게놈 지도'를 완성한 스타 과학자인 크레이그 벤터(Craig Venter) 박사는 역사적인 세계해양탐사(GOS) 5) 를 2003년에 시작하였다. 그는 자신이 소유한 요트를 개조하여 두 차례에 걸쳐 전 세계 해역을 대상으로 해양미생물 탐사항해를 벌였다. 이 탐사에서 매 200마일마다 200~400리터의 해수를 채취하여 DNA 해독을 통해, 약 600만 개의 새로운 유전자와 해수 1L당 10종~200종 정도의 신종 미생물이 존재함을 발견하여 해양에서의 미생물 다양성을 보여 주었다. 세계 각국에서는 나고야의정서의 발효로 갈수록 치열해질 유용 해양생물자원 확보 전쟁에 대응하고 안정적인 생물자원확보를 위하여 극지, 심해, 공해상 등지에서 해양생물자원탐사를 진행하고 있다. 또한 배양이 어려운 난배양성 해양미생물의 분리 및 배양에 대한 연구가 활발히 진행되고 있다. 벤터 박사의 탐사에서도 알 수 있듯이 일반적으로 배양될 수 있는 미생물은 전체의 1% 정도밖에 되지 않는다. 그리하여 해양미생물 유래의 새로운 천연물의 발견을 위하여 배양이 불가능했거나 어려운 미생물의 효과적인 배양을 위한 방법 개발에 많은 관심이 쏠리고 있다. 해양미생물유래 신규 천연물의 개발은 새로운 유용 해양미생물의 발견뿐만 아니라 다양한 새로운 방법들의 개발에 의해서도 이루어질 수 있다. 이러한 방법들로는 구조분석 장비의 고도화, 고효율활성검색(HTS )6), 메타게놈(metagenome), 대사체학(metabolomics), 유전체학(genomics), 조합 생합성 방법(combinatorial biosynthesis),합성생물학(synthetic biology) 등의 여러 가지 방법 및 전략들이 연구되고 있다. 해양환경 중에 존재하는 대부분의 미생물들은 실험실에서 쉽게 배양되지 않는다. 따라서, 어떤 환경에 존재하는 미생물의 전체 유전체들을 연구할 수 있는 메타게놈은 해양미생물유래의 새로운 천연물 발견에 적합하다. 해양메타게놈의 연구대상으로는 해수의 미생물 군집, 해면동물 및 무척추동물의 공생미생물 군집, 광합성세균 군집, 심해 열수분출구 군집 등으로 점차 확대되어 가고 있다. 미생물이 생산하는 다양한 2차대사산물들은 염색체에 있는 여러 개의 생합성 관련 유전자들, 즉 유전자 클러스터로부터 생산된다. 현재 450개 이상의 미생물 유래 천연물 유전자 클러스터가 알려져 있는데, 유전체학 연구를 통해 천연물 생합성에 관여하는 유전자 클러스터의 연구가 미생물 유래 새로운 천연물 발견에 적용되고 있다. 일반적으로 천연물은 구조가 복잡하여 화학합성을 통한 유도체 생산이 어려운데,이러한 문제점을 극복하기 위하여 조합 생합성 방법을 이용하여 천연물의 화학적 다양성을 증가시키는 연구도 활발히 진행되고 있다. 또한 합성생물학의 빠른 발전은 이미 알려진 활성화합물의 대량생산 또는 비활성 생합성 유전자(silent gene cluster)의 활성화를 통한 신규 천연물의 발굴에 좋은 연구 방법으로 활용될 수 있다.
3.2 KIOST 연구사업에 미치는 영향
최근 핵자기공명장치(NMR)7) 및 질량분석기(MS)8) 와 같은 구조분석 기기의 발달에 힘입어 해양생물체내에 미량으로 존재하는 활성물질의 구조분석 기술이 눈부시게 발전하였다. 해양천연물화학은 해양생물체내에 존재하는 대사물질들을 분리, 정제하고 이들 물질들의 활성 및 구조를 규명하는 것이 연구의 중요한 부분이다. 선진국에서는 분석장비의 고도화를 통하여 아주 미량의 물질에 대해서도 활성 및 구조를 밝혀 지적재산권를 선점하고 있다. 신약소재 개발 역량을 강화하고 활성물질의 원천특허를 확보하기 위해 NMR 및 MS 등과 같은 분석장비의 고도화가 꼭 필요한 시점이다.해양미생물자원 탐사 분야에서는 한국해양과학기술원이 오랜 연구를 통하여 많은 해양미생물자원을 발굴하여왔다. ‘서태평양 종합대양연구’를 통하여 서태평양해역 해양 탐사를 실시하여 심해시료를 확보하였고, 심해 미생물의 분리 및 미생물다양성 연구를 진행하였다.“해양방선균으로부터 항암물질 개발”사업을 통하여 북극, 심해, 열대지방, 국내 연근해 등에서 2,000여종의 해양방선균을 분리/보존하였으며, 전술하였던 스트렙토클로린 등의 다수의 활성물질을 발굴하였다. 뿐만 아니라 “해외 해양생물자원 개발 및 활용기반 구축” 사업(2009~2017, 연구책임자 이희승)을 통하여 7,000여점의 해양미생물을 마이크로네시아, 필리핀, 베트남, 방글라데시 등 해외 해양생물자원 및 퇴적토로부터 분리/보존하였다. 또한 “인도양 중앙해령대 심해열수공 생명시스템 이해”사업(2017~, 연구책임자 김동성)을 통하여 심해 열수분출공 주변의 다양한 생물 및 심해 샘플들로부터 심해미생물을 분리할 예정이다.문제는 기존의 연구사업에서 분리한 해양미생물 및 앞으로 새롭게 시작할 연구사업을 통하여 확보되어질 많은 해양미생물들 중에서 엄청난 파급효과를 가져올 보석을 어떻게 찾느냐 하는 일이다. 수없이 많은 해양미생물들 중에서 유용 균주를 빠르게 선별하기 위하여서는 고효율활성검색(HTS) 시스템의 도입, 분석장비의 고도화 등이 시급하며, 대사체학이나 메타게놈, 합성생물학 전공자의 인력보충과 육성도 절실하다고 할 수 있다.이제 전 세계 바다를 대상으로 탐사할 수 있는 6천톤급 종합연구선 이사부호를 통하여 심해 열수분출공의 주변 생물시료 및 다양한 해양시료를 확보할 수 있게 되었으며, 이와 함께 최신 연구장비 및 효율적인 연구 인프라를 갖추게 될 때에 바다 속에 숨겨져 있는 해양미생물이라는 보물창고를 우리 손으로 열게 될 날이 멀지 않게 될 것이다.
5) Global Ocean Sampling Expedition.
6) High-Throughput Screening: 다수의 물질에 대한 분석을 고속으로 수행하는 고효율의 물질 탐색 방법.
7) Nuclear Magnetic Resonance: 물질의 구조해석에 있어서 가장 폭넓게 사용되는 분석 장비.
4. 결론 및 정책 제언
해양은 생물의 탄생과 진화의 보금자리이며, 해양미생물은 지구 생물다양성의 원천으로서 지속적으로 이용 가능한 해양의 핵심 자원이다. 아직 1%밖에 알려지지 않은 해양미생물들은 무한한 가치를 가지고 있다. 우리가 사용하고 있는 대부분의 항생제와 많은 항암제가 육상미생물에서 나왔듯이, 해양미생물은 21세기의 의약품의 보고가 될 것이라고 예상되고 있다. 따라서 해양미생물의 다양성을 이해하고 이들이 생산하는 유용물질의 활용 가능성을 밝히는 것은 우리나라의 해양바이오 산업 발전과 관련 산업의 활성화를 위해 반드시 필요하다. 경제협력개발기구(OECD)9)는 2030년경 바이오기술이 글로벌 경제의 변화를 이끌 바이오 경제로 진입할 것으로 전망하였으며, 전문가들은 바이오 혁명이 ICT, 화학, 생물학, 물리학, 수학 등과의 융합을 통해 제 2차 바이오혁명을 이끌어 바이오 기반의 경제시대로 이어질 것으로 내다보고 있다. 해양미생물이 생산하는 천연물의 연구는 자원으로서의 해양미생물의 가치를 파악하는 연구로써 구조분석장비, 고효율활성검색, 차세대염기서열분석(NGS)10) , 메타게놈 및 단일세포유전체 분석기법 등의 기술 발전과 함께 빠르게 발전하고 있다. 과거와는 달리 염기서열 분석기술의 발달로 유전체 정보에 기반하여 해양미생물 자원의 숨겨진 잠재력, 즉 유용물질 생산 가능성을 평가하는 것이 훨씬 쉬워졌다. 해양미생물에 대한 연구는 신종 미생물의 발견과 같은 자원 확보 기술로부터 신약 개발, 바이오에너지 생산, 유용 효소의 산업적 응용 등의 다양한 분야로 확장되어 해양바이오 시대를 선도하는 핵심 연구 분야가 될 것이다. 신약개발은 인구 고령화에 따라서 지속적인 수요 증가가 전망되는 미래산업으로 전 세계적으로 R&D 투자가 빠르게 증가하고 있다. 우리나라가 글로벌 제약강국으로 도약하기 위해서는 연구비의 지원 확대, 생물자원 개발을 위한 인프라 지원 및 인력육성 등이 지속적으로 이뤄져야 한다. 해양미생물자원의 확보/관리 기반시스템 구축에 국가의 체계적인 지원과 관련 기관/기업들의 연구투자가 지속된다면 국내기술에 의한 해양미생물 유래 천연물신약 개발이 국제경쟁력을 갖추고 세계적인 신약이 출현할 날 또한 멀지 않을 것이다.
8) Mass Spectrometer: 시료를 이온화하여 생성된 이온을 질량/전하비에 의해서 어떤 물질의 질량을 분석하는 장비.
9) Organization for Economic Cooperation and Development.
10) Next Generation Sequencing: 한 생물의 유전자 정보 전체를 빠르게 읽어낼 수 있는 염기서열 분석 기술.
참고문헌
Berdy, Y. (2012). Thoughts and facts about antibiotics: Where we are now and where we are heading. J. Antibiot., 65: 385-395.
Bouchie, A. (2016). White House unveils National Microbiome Initiative. Nature Biotech., 34, 580.
Huang, T. and Lin, S. (2017). Microbial Natural Products: A Promising Source for Drug Discovery. J. Appl. Microbiol. Biochem., 2(1): 1-3.
Li, X., Qin, L. (2005). Metagenomics-based drug discovery and marine microbial diversity. Trends Biotechnol. 23, 539-543.
Martins, A., Vieira, H., Gaspar, H., Santos, S. (2016). Marketed Marine Natural Products in the Pharmaceutical and Cosmeceutical Industries: Tips for Success. Mar. Drugs, 12, 1066-1101.
McCarthy, P.J., Pomponi, S. A. (2004). A search for new Pharmaceutical Drugs from marine organisms. Marine Biomed. Res. 1-2.
Mehbub, M. F., Lei, J., Franco, C., Zhang, W. (2014). Marine Sponge Derived Natural Products between 2001 and 2010: Trends and Opportunities for Discovery of Bioactives. Mar. Drugs, 12, 4539-4577.
Newman, D.J. and Cragg, G.M. (2016). Natural products as sources of new drugs from 1981 to 2014. J. Nat. Prod., 79, 629-661.
Xiong, Z.Q., Wang, J.F., Hao, Y.Y., Wang, Y. (2013). Recent advances in the discovery and development of marine microbial natural products. Mar. Drugs, 11, 700-717.
 온라인 역사관
온라인 역사관